Aldehyd masłowy
| |||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||
| Ogólne informacje | |||||||||||||||||||||||||||||||||||||
| Wzór sumaryczny |
C4H8O | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Inne wzory |
CH | ||||||||||||||||||||||||||||||||||||
| Masa molowa |
72,11 g/mol | ||||||||||||||||||||||||||||||||||||
| Wygląd |
bezbarwna ciecz o nieprzyjemnym, gryzącym zapachu[1] | ||||||||||||||||||||||||||||||||||||
| Identyfikacja | |||||||||||||||||||||||||||||||||||||
| Numer CAS | |||||||||||||||||||||||||||||||||||||
| PubChem | |||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | |||||||||||||||||||||||||||||||||||||
Aldehyd masłowy, butanal – organiczny związek chemiczny z grupy aldehydów. Występuje naturalnie w niewielkich ilościach w olejkach eterycznych i roślinach[1].
Otrzymywanie
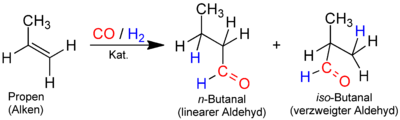
[edytuj | edytuj kod]Zasadniczą metodą otrzymywania aldehydu masłowego stosowaną obecnie w przemyśle jest hydroformylowanie propenu:
Stosuje się przy tym katalizatory homogeniczne będące hydrydokarbonylkami metali przejściowych[12], np. kompleksy hydrydokarbonylorodu(I)[13]. Tą metodą otrzymuje się mieszaninę aldehydu masłowego i aldehydu izomasłowego o czystości 90–98%[12]. Roczna produkcja butanalu wynosi około 6,8×106 ton i opiera się głównie na powyższej metodzie[1].
Przed opracowaniem metody hydroformylowania najczęściej stosowana była kondensacja aldolowa aldehydu octowego do aldehydu krotonowego, a następnie jego katalityczne uwodornienie[14]. Inną metodą, niestosowaną na skalę przemysłową, jest odwodornienie butanolu przeprowadzane w fazie gazowej z katalizatorem heterogenicznym opartym na miedzi z dodatkami cynku lub chromu. Niewielkie ilości butanalu powstają także w syntezie Fischera-Tropscha[14].
Właściwości
[edytuj | edytuj kod]W temperaturze pokojowej jest łatwopalną cieczą o ostrym, gryzącym zapachu, podrażnia oczy i skórę oraz układ oddechowy[9]. Stosunkowo słabo rozpuszcza się w wodzie, natomiast miesza się z wieloma rozpuszczalnikami organicznymi[1]. Pod wpływem śladowych ilości kwasów ulega trimeryzacji, czemu można zapobiec dodatkiem zasady (np. trietanoloaminy). W kontakcie z powietrzem łatwo ulega utlenieniu do kwasu masłowego i z tego względu wymaga przechowywania w atmosferze gazu obojętnego[15].
Zastosowanie
[edytuj | edytuj kod]Najważniejszą reakcją stosowaną w przemyśle jest kondensacja aldehydu masłowego z zasadowym katalizatorem, w wyniku której powstaje 2-etyloheksanal, który następnie poprzez uwodornienie przekształcany jest do 2-etyloheksanolu – związku służącego do otrzymywania ftalanu dioktylu (DOP), plastyfikatora poli(chlorku winylu) (PCW)[16].
Stosuje się go również do otrzymywania innych związków, głównie od cztero- do ośmiowęglowych[1], a także gum i żywic syntetycznych[17][18].
Przypisy
[edytuj | edytuj kod]- ↑ a b c d e f g Cornils, Fisher i Kohlpaintner 2003 ↓, s. 1.
- ↑ a b c d Haynes 2009 ↓, s. 3-72.
- ↑ Haynes 2009 ↓, s. 16-42.
- ↑ Butyraldehyde, [w:] PubChem [online], United States National Library of Medicine, CID: 261 [dostęp 2022-07-10] (ang.).
- ↑ Farmakopea Polska X, Polskie Towarzystwo Farmaceutyczne, Warszawa: Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych, 2014, s. 4276, ISBN 978-83-63724-47-4.
- ↑ a b Haynes 2009 ↓, s. 6-55.
- ↑ Haynes 2009 ↓, s. 9-53.
- ↑ butyraldehyde, [w:] Classification and Labelling Inventory, Europejska Agencja Chemikaliów [dostęp 2015-03-28] (ang.).
- ↑ a b Butyroaldehyd (nr 418102) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Polski. [dostęp 2022-07-10]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ Butyraldehyde (nr 418102) (ang.) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Stanów Zjednoczonych. [dostęp 2013-03-17]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ a b Haynes 2009 ↓, s. 16-17.
- ↑ a b Cornils, Fisher i Kohlpaintner 2003 ↓, s. 2.
- ↑ Fred H. Jardine, Rhodium: Inorganic and Coordination Chemistry, [w:] Encyclopedia of Inorganic Chemistry, R. Bruce King, wyd. 2, t. I, Chichester: Wiley, 2005, s. 3, ISBN 978-0-470-86078-6.
- ↑ a b Cornils, Fisher i Kohlpaintner 2003 ↓, s. 4.
- ↑ Cornils, Fisher i Kohlpaintner 2003 ↓, s. 5.
- ↑ Cornils, Fisher i Kohlpaintner 2003 ↓, s. 6.
- ↑ Encyclopedic dictionary of polymers, Jan W. Gooch (red.), t. 1, New York: Springer, 2011, s. 105, DOI: 10.1007/978-1-4419-6247-8, ISBN 978-1-4419-6246-1.
- ↑ Butyraldehyde, [w:] Merck Index. An Encyclopedia of Chemicals, Drugs, and Biologicals, wyd. 13, Whitehouse Station: Merck & Company, 2001, ISBN 0-911910-13-1, OCLC 224225657 (ang.).
Bibliografia
[edytuj | edytuj kod]- David R. Lide (red.), CRC Handbook of Chemistry and Physics, wyd. 90, Boca Raton: CRC Press, 2009, ISBN 978-1-4200-9084-0 (ang.).
- Roy Cornils, Richard W. Fisher, Christian Kohlpaintner, Butanals, [w:] Ullmann’s Encyclopedia of Chemical Industrial Chemistry, wyd. 6, Weinheim: Viley-VCH, 2003, DOI: 10.1002/14356007, ISBN 978-3-527-30385-4.